勉強ネタ 2018年9月5日 銅から酸素を奪うやつ。炭素。(酸化還元の問題②)
昨日の続きです。
[box class=”blue_box” title=”酸化還元の計算問題”]
酸化銅6.00gに炭素の粉末0.15gを混ぜ加熱すると0.55gの二酸化炭素が発生。
同様に0.30gの炭素で1.10g、0.45gで1.65g、0.60gで1.65g、0.75gで1.65gの二酸化炭素が発生。
では酸化銅5.40gに0.36gの炭素粉末を混ぜると何gの二酸化炭素が発生するか?
[/box]
銅と酸素が遊んでいるところに
0.15gの炭素がやってくると、0.40gの酸素が奪われる。
(炭素と酸素で出来上がった二酸化炭素が0.55gでそのうち炭素は0.15gなので引き算をすれば奪われた酸素がわかる)
炭素 + 酸素 → 二酸化炭素
同じように計算すると
炭素0.30gで、0.80gの酸素が、炭素0.45gで1.2gの酸素が奪われていることがわかる。
昨日説明した通り、炭素が2倍3倍と増えると
奪われる酸素も2倍3倍と比例して増えている。
問題なのは次から。
0.60gと0.75gの炭素、更に炭素の量を増やしたにもかかわらず
発生した二酸化炭素の量が1.65gと
なにもかわっていない。
二酸化炭素の量が増えていないということは
炭素が酸素を奪えていない証拠。
ここで、昨日の話を思い出してほしい。
炭素を増やせばそれに比例して酸素も奪えるが、ある一定の量を超えると、酸素が抵抗し始める。
そう、酸素がこれ以上炭素のところになんていってやるもんかと
抵抗をし始めたのだ。
ここまでを図でまとめるとこんな感じ。
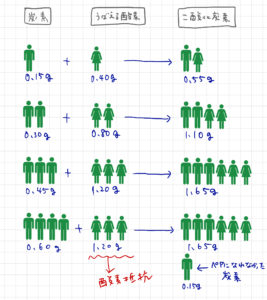 0.45gの炭素までは、奪える酸素も比例して増えていっていることがわかるが
その先、どんなに炭素が増えても、奪える酸素はかわらないことが
わかるだろう。
ふぅ。。。
説明が難しい。。。
さて、ここまできてやっと問題が解ける。
0.36gの炭素が来たら、何g二酸化炭素が発生するか?と聞かれている。
0.45gの炭素までは、比例して酸素を奪えるわけだから
0.15g : 0.40g = 0.36g : x
この比例式を解いて
x=0.96g(奪われた酸素)
0.36g(炭素) + 0.96g(奪われた酸素) = 1.32g
発生した二酸化炭素は1.32gが正解。
いろいろと説明をしたが
結局単純な比例式で解けてしまった(;´∀`)
炭素の量が酸素抵抗ゾーンに絡む問題ではないので
しかたないか。。。
なんかつかれた。。。(;´∀`)
0.45gの炭素までは、奪える酸素も比例して増えていっていることがわかるが
その先、どんなに炭素が増えても、奪える酸素はかわらないことが
わかるだろう。
ふぅ。。。
説明が難しい。。。
さて、ここまできてやっと問題が解ける。
0.36gの炭素が来たら、何g二酸化炭素が発生するか?と聞かれている。
0.45gの炭素までは、比例して酸素を奪えるわけだから
0.15g : 0.40g = 0.36g : x
この比例式を解いて
x=0.96g(奪われた酸素)
0.36g(炭素) + 0.96g(奪われた酸素) = 1.32g
発生した二酸化炭素は1.32gが正解。
いろいろと説明をしたが
結局単純な比例式で解けてしまった(;´∀`)
炭素の量が酸素抵抗ゾーンに絡む問題ではないので
しかたないか。。。
なんかつかれた。。。(;´∀`)
 0.45gの炭素までは、奪える酸素も比例して増えていっていることがわかるが
その先、どんなに炭素が増えても、奪える酸素はかわらないことが
わかるだろう。
ふぅ。。。
説明が難しい。。。
さて、ここまできてやっと問題が解ける。
0.36gの炭素が来たら、何g二酸化炭素が発生するか?と聞かれている。
0.45gの炭素までは、比例して酸素を奪えるわけだから
0.15g : 0.40g = 0.36g : x
この比例式を解いて
x=0.96g(奪われた酸素)
0.36g(炭素) + 0.96g(奪われた酸素) = 1.32g
発生した二酸化炭素は1.32gが正解。
いろいろと説明をしたが
結局単純な比例式で解けてしまった(;´∀`)
炭素の量が酸素抵抗ゾーンに絡む問題ではないので
しかたないか。。。
なんかつかれた。。。(;´∀`)
0.45gの炭素までは、奪える酸素も比例して増えていっていることがわかるが
その先、どんなに炭素が増えても、奪える酸素はかわらないことが
わかるだろう。
ふぅ。。。
説明が難しい。。。
さて、ここまできてやっと問題が解ける。
0.36gの炭素が来たら、何g二酸化炭素が発生するか?と聞かれている。
0.45gの炭素までは、比例して酸素を奪えるわけだから
0.15g : 0.40g = 0.36g : x
この比例式を解いて
x=0.96g(奪われた酸素)
0.36g(炭素) + 0.96g(奪われた酸素) = 1.32g
発生した二酸化炭素は1.32gが正解。
いろいろと説明をしたが
結局単純な比例式で解けてしまった(;´∀`)
炭素の量が酸素抵抗ゾーンに絡む問題ではないので
しかたないか。。。
なんかつかれた。。。(;´∀`) 

